Bộ Y tế phạt doanh nghiệp Ấn Độ sản xuất thuốc không đạt chất lượng
(VietQ.vn) - Cục Quản lý Dược - Bộ Y tế vừa ban hành quyết định xử phạt vi phạm hành chính và yêu cầu tiêu hủy các sản phẩm thuốc Cefpodoxime Proxetil Tablets USP do Công ty Syncom Formulaion - Ấn Độ sản xuất, đăng ký, không đạt chất lượng.
Bộ trưởng Y tế nhận định về 'trói không chặt' việc mua bán thuốc
Thu hồi thuốc kém chất lượng do Công ty Tân Xuân Dược đăng ký
Thu hồi thuốc viên nén Doxferxime và thuốc nhỏ mắt Dexacol
Cụ thể, Cục Quản lý Dược ban hành Quyết định số 611/QĐ-XPHC ngày 13/11/2015 về việc xử phạt hành chính về thuốc đối với Công ty Syncom Formulaion - India. Do sản xuất, cung cấp thuốc viên nén Cefpodoxime Proxetil Tablets USP 100mg SĐK VN-14818-12, lô XC 4010, NSX: 03/01/2014, HD: 02/01/2017 và thuốc viên nén Cefpodoxime Proxetil Tablets USP 200mg SĐK VN-14819-12, lo XD 4009, NSX: 10/6/2014, HD: 09/6/2017 không đạt yêu cầu chất lượng mức độ 3 theo quy định của pháp luật.
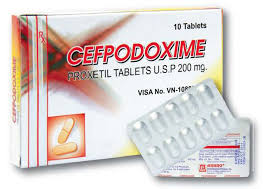 Thu hồi Cefpodoxime Proxetil Tablets USP kém chất lượng
Thu hồi Cefpodoxime Proxetil Tablets USP kém chất lượng
Công ty này có địa chỉ tại số 7 Nirjai Estate, off. Mahakali Caves Road, Andheri (East), India. Doanh nghiệp này chuyên cung cấp thành phẩm tân dược, nguyên liệu làm thuốc, thuốc có nguồn gốc từ dược liệu.
Sai phạm của Công ty Syncom Formulaion - India theo điểm C khoản 2 điều 39 của Nghị định số 176/2013/NĐ-CP ngày 14/11/2013 của Chính phủ quy định về xử phạt vi phạm hành chính trong lĩnh vực y tế. Trong vòng 12 tháng, Công ty Syncom Formulaion có 3 lô thuốc vi phạm chất lượng mức độ 3 theo quy định của pháp luật.

Công ty Syncom Formulaion - India sản xuất thuốc kém chất lượng
Công ty Syncom Formulaion bị phạt 50 triệu đồng và phải phối hợp với các cơ quan liên quan thu hồi và hủy thuốc viên nén Cefpodoxime Proxetil Tablets USP 100mg SĐK VN-14818-12, lô XC 4010, NSX: 03/01/2014, HD: 02/01/2017 và thuốc viên nén Cefpodoxime Proxetil Tablets USP 200mg SĐK VN-14819-12, lo XD 4009, NSX: 10/6/2014, HD: 09/6/2017 không đạt yêu cầu chất lượng mức độ 3 theo quy định tại Thông tư 09/2010/TT- BYT ngày 28/4/21010 của Bộ Y tế.
Ngoài mức phạt trên, công ty này còn bị tước quyền sử dụng giấy phép hoạt động về thuốc và nguyên liệu làm thuốc do Bộ Y tế cấp trong thời hạn 6 tháng kể từ ngày bị xử phạt.