Thu hồi gel sát khuẩn của Công ty Blaine Labs do nhiễm vi khuẩn
(VietQ.vn) - Công ty Blaine Labs, Inc. đã ra thông báo thu hồi tự nguyện trên toàn nước Mỹ đối với các sản phẩm gel chăm sóc vết thương Revitaderm và Tridergel sau khi phát hiện nhiễm vi khuẩn, tiềm ẩn nguy cơ nhiễm trùng.
Thu hồi phô mai sữa tươi RAW FARM do nghi nhiễm E.coli
Thu hồi khẩn lô thuốc Pentovas điều trị viêm gan B mạn tính do không đạt chuẩn
Thu hồi toàn quốc lô thuốc giảm đau, kháng viêm Aceclofenac STELLA 100mg
Thu hồi socola của Công ty Gear Isle do chứa thành phần không được khai báo
Theo Cục Quản lý Thực phẩm và Dược phẩm Hoa Kỳ (FDA), các sản phẩm bị ảnh hưởng gồm gel sát khuẩn vết thương mang thương hiệu Revitaderm và Tridergel, dạng chai 1 ounce (khoảng 28,3 gram) và tuýp 3 ounce (khoảng 85 gram), chứa hoạt chất Benzalkonium Chloride 0,1%. Các sản phẩm này được phân phối tới các cơ sở y tế như phòng khám, không bán lẻ trực tiếp trên thị trường.
Cụ thể, các mẫu kiểm nghiệm đã phát hiện sự hiện diện của vi khuẩn Lysinibacillus fusiformis – một loại vi khuẩn hình thành bào tử, tồn tại phổ biến trong môi trường tự nhiên. Dù thường được đánh giá có độc lực thấp với người khỏe mạnh, vi khuẩn này có khả năng sống sót trong điều kiện bất lợi và có thể trở thành tác nhân gây bệnh cơ hội.
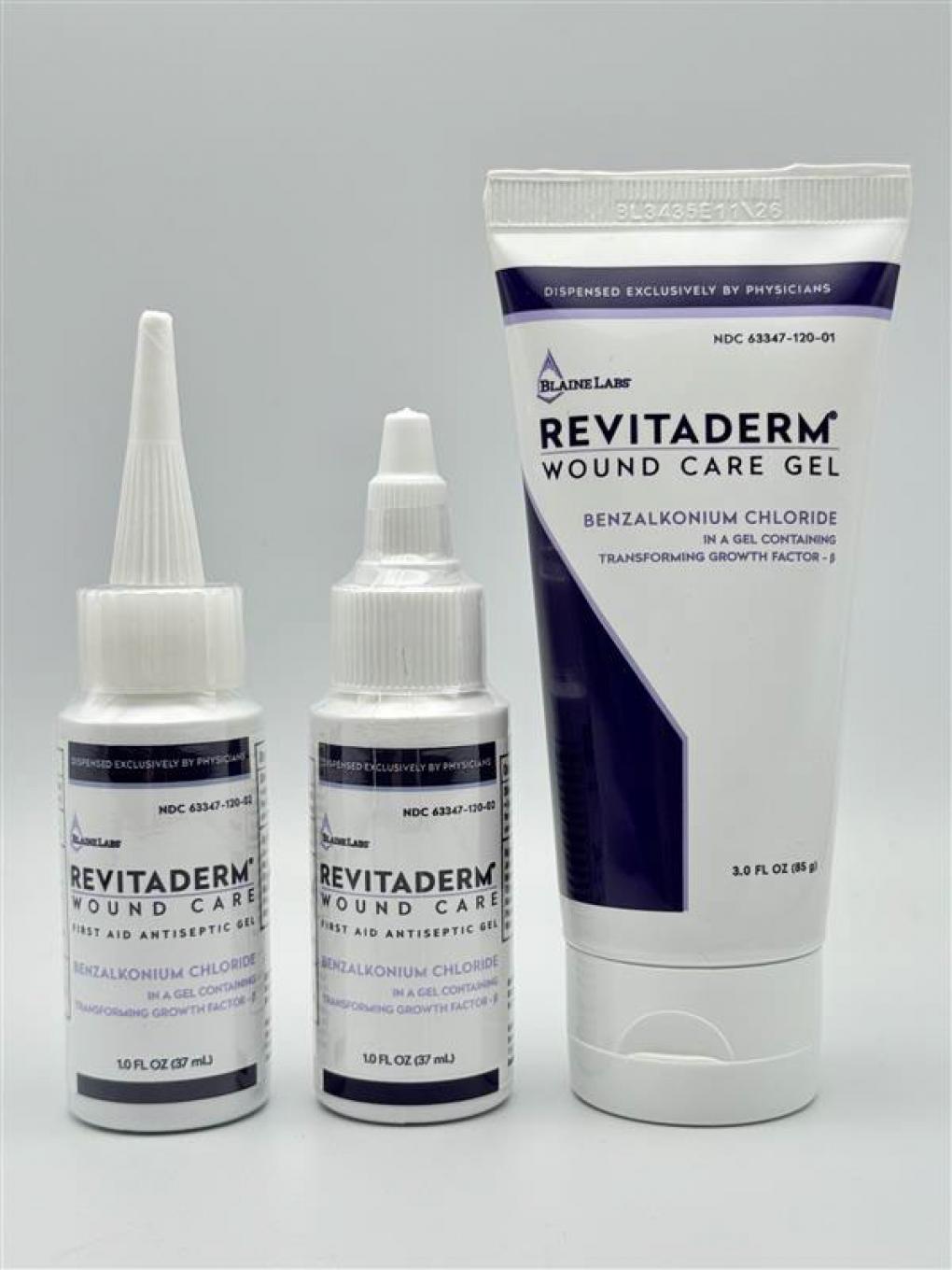 Sản phẩm nằm trong diện thu hồi. Ảnh: FDA
Sản phẩm nằm trong diện thu hồi. Ảnh: FDA
Đáng lưu ý, những người có vết thương hở, tổn thương hàng rào bảo vệ da hoặc hệ miễn dịch suy giảm (như người cao tuổi, bệnh nhân tiểu đường, trẻ nhỏ) có nguy cơ cao bị nhiễm trùng, kích ứng da hoặc chậm lành vết thương khi sử dụng sản phẩm nhiễm khuẩn.
Trong các trường hợp nghiêm trọng, đặc biệt ở người suy giảm miễn dịch, nhiễm khuẩn có thể tiến triển thành các biến chứng nguy hiểm như viêm nội tâm mạc hoặc nhiễm trùng hệ thần kinh trung ương, đe dọa tính mạng.
Đại diện Blaine Labs cho biết, tính đến thời điểm hiện tại chưa ghi nhận bất kỳ báo cáo nào về phản ứng bất lợi liên quan đến các sản phẩm thuộc diện thu hồi. Tuy nhiên, việc thu hồi được thực hiện như một biện pháp phòng ngừa nhằm đảm bảo an toàn tối đa cho người sử dụng.
Các lô sản phẩm bị ảnh hưởng được xác định thông qua số lô và hạn sử dụng in trên bao bì, bao gồm các mã như BL3608, BL3435 và BL3525, với hạn dùng từ năm 2026 đến 2028.
Công ty khuyến cáo các cơ sở y tế và người sử dụng cần rà soát tồn kho, ngừng ngay việc sử dụng và phân phối các sản phẩm thuộc lô bị ảnh hưởng. Các sản phẩm còn lại cần được cách ly và liên hệ với nhà sản xuất để thực hiện quy trình thu hồi. Blaine Labs cũng đã chủ động thông báo tới các phòng khám qua thư và điện thoại, đồng thời phối hợp thu hồi toàn bộ sản phẩm chưa sử dụng.
Tại Việt Nam, việc quản lý chất lượng thuốc và sản phẩm chăm sóc vết thương được thực hiện theo hệ thống quy định chặt chẽ. Cụ thể, Luật Dược 2016 yêu cầu thuốc lưu hành phải đáp ứng đầy đủ tiêu chuẩn chất lượng, bao gồm các chỉ tiêu về vô khuẩn hoặc giới hạn vi sinh tùy theo dạng bào chế.
Bên cạnh đó, Thông tư 11/2018/TT-BYT quy định các chế phẩm dùng ngoài phải kiểm soát nghiêm ngặt chỉ tiêu vi sinh, không được chứa vi sinh vật gây bệnh và phải nằm trong giới hạn cho phép. Các yêu cầu kỹ thuật cụ thể được quy định tại Dược điển Việt Nam V, trong đó nêu rõ giới hạn vi sinh đối với thuốc không vô khuẩn, phương pháp thử và yêu cầu không có các vi khuẩn gây bệnh phổ biến trong chế phẩm dùng ngoài da.
Đồng thời, việc sản xuất phải tuân thủ nguyên tắc WHO-GMP nhằm kiểm soát môi trường, quy trình và ngăn ngừa nhiễm vi sinh, nhiễm chéo. Ở cấp độ khu vực, Việt Nam cũng áp dụng ASEAN Guidelines on Microbial Limits để hài hòa quy định về giới hạn vi sinh đối với dược phẩm không vô khuẩn. Sau khi lưu hành, các rủi ro liên quan đến chất lượng, bao gồm nguy cơ nhiễm vi sinh, tiếp tục được giám sát thông qua Hệ thống cảnh giác dược Việt Nam. Những quy định này cho thấy kiểm soát vi sinh là yêu cầu bắt buộc đối với các sản phẩm sử dụng trực tiếp trên vết thương, nhằm bảo đảm an toàn cho người sử dụng và hạn chế tối đa nguy cơ nhiễm khuẩn.
Duy Trinh

















