Mỹ thu hồi thuốc điều trị ung thư của Sun Pharma do nguy cơ lẫn mảnh thủy tinh
(VietQ.vn) - Công ty dược phẩm Sun Pharmaceutical Industries (Sun Pharma) đã phát đi thông báo thu hồi tự nguyện trên toàn nước Mỹ đối với một lô thuốc tiêm DOXOrubicin Hydrochloride Liposome Injection 50mg/25 mL sau khi phát hiện nguy cơ tồn tại các mảnh thủy tinh trong lọ thuốc.
Mỹ thu hồi nhiều sản phẩm ăn vặt của Công ty John B. Sanfilippo & Son do nguy cơ nhiễm khuẩn
Viện thẩm mỹ Khơ Thị bị xử phạt, buộc thu hồi và đưa mỹ phẩm vi phạm ra khỏi lãnh thổ Việt Nam
Cảnh báo loạt sản phẩm bị thu hồi tại nước ngoài có nguy cơ ảnh hưởng tới người tiêu dùng Việt
Thu hồi khẩn cấp lô sữa A2 Platinum Premium do nhiễm khuẩn cereulide
Theo Cục Quản lý Thực phẩm và Dược phẩm Hoa Kỳ (FDA), đợt thu hồi được thực hiện đối với lô thuốc mang số HAG2581B, hạn dùng đến ngày 31/5/2027, gồm 675 lọ thuốc phân phối tại thị trường Mỹ.
Sun Pharma cho biết, nguyên nhân thu hồi xuất phát từ việc phát hiện các mảnh thủy tinh trong một số lọ thuốc trong quá trình sản xuất. Đây là loại thuốc tiêm truyền tĩnh mạch nên nguy cơ gây ảnh hưởng nghiêm trọng đến sức khỏe người bệnh nếu các hạt thủy tinh đi vào cơ thể.
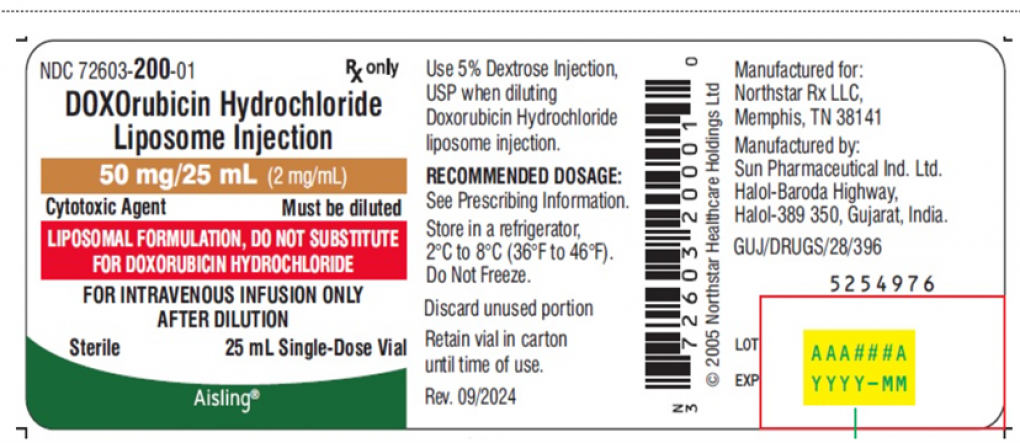 Nhãn sản phẩm thuộc diện thu hồi. Ảnh: FDA
Nhãn sản phẩm thuộc diện thu hồi. Ảnh: FDA
Theo cảnh báo của doanh nghiệp, các mảnh thủy tinh có thể gây kích ứng cục bộ, sưng viêm tại vị trí truyền. Trong những trường hợp nghiêm trọng hơn, dị vật có thể làm tắc mạch máu hoặc gây hình thành cục máu đông đe dọa tính mạng người bệnh. Tuy nhiên, đến thời điểm hiện tại, Sun Pharma cho biết, chưa ghi nhận báo cáo về phản ứng bất lợi liên quan đến lô thuốc bị thu hồi.
DOXOrubicin Hydrochloride Liposome Injection là thuốc hóa trị dạng liposome, được chỉ định điều trị ung thư buồng trứng, sarcoma Kaposi liên quan đến AIDS và bệnh đa u tủy. Sản phẩm được đóng gói trong lọ thủy tinh đơn liều 25 mL, dung dịch màu đỏ bán trong suốt, mang nhãn Aisling với mã NDC 72603-200-01.
Sun Pharma đang phối hợp với các nhà phân phối, bệnh viện và cơ sở y tế để thu hồi toàn bộ số thuốc thuộc lô bị ảnh hưởng. Công ty yêu cầu các đơn vị phân phối, nhà thuốc, bệnh viện và người sử dụng ngừng dùng sản phẩm ngay lập tức, đồng thời hoàn trả hoặc tiêu hủy theo hướng dẫn.
FDA cho biết, việc thu hồi được tiến hành với sự giám sát của cơ quan này. Người bệnh nếu gặp các dấu hiệu bất thường liên quan đến việc sử dụng thuốc được khuyến cáo liên hệ bác sĩ hoặc cơ sở y tế để được hỗ trợ kịp thời.
Trong lĩnh vực sản xuất thuốc tiêm vô trùng, việc kiểm soát tiểu phân ngoại lai, bao gồm mảnh thủy tinh, là yêu cầu đặc biệt nghiêm ngặt do nguy cơ ảnh hưởng trực tiếp đến an toàn người bệnh. Các tiêu chuẩn quốc tế như hướng dẫn Thực hành sản xuất tốt thuốc (GMP) của Tổ chức Y tế Thế giới (WHO), tiêu chuẩn của FDA Hoa Kỳ và Dược điển Hoa Kỳ (USP) đều yêu cầu thuốc tiêm phải được kiểm tra chặt chẽ về tiểu phân nhìn thấy và không nhìn thấy trước khi lưu hành.
Liên quan đến quản lý chất lượng và an toàn đối với thuốc tiêm vô trùng, Việt Nam hiện áp dụng nhiều tiêu chuẩn, quy chuẩn và quy định kỹ thuật như TCVN 6153:1996 về yêu cầu kỹ thuật đối với thuốc tiêm liên quan đến độ trong và tiểu phân cơ học; Dược điển Việt Nam V (TCVN I-3:2017) quy định các chỉ tiêu chất lượng đối với thuốc tiêm và chế phẩm tiêm truyền; TCVN 8689-1:2011 (ISO 14644-1) về phân loại độ sạch không khí trong phòng sạch sản xuất dược phẩm. Bên cạnh đó, hoạt động sản xuất thuốc còn phải tuân thủ Thông tư 35/2018/TT-BYT về Thực hành tốt sản xuất thuốc (GMP) và Thông tư 11/2018/TT-BYT quy định về chất lượng thuốc, nguyên liệu làm thuốc.
Duy Trinh


















