Bộ Y tế không ủng hộ tiêm vaccine chưa được cấp phép cho người dân
(VietQ.vn) - Bộ Y tế ủng hộ các tỉnh tham gia thử nghiệm lâm sàng để đánh giá hiệu quả an toàn của vaccine Covid-19 Nanocovax, song không dùng để "tiêm thí điểm".
Vaccine ngừa Covid-19 của Pfizer và Moderna tăng giá tại thị trường EU
Hiệu quả vaccine Covid-19 dạng hít và xịt mũi - niềm hy vọng mới cho thế giới chống đại dịch
Chân dung nhà khoa học nữ đứng sau thành công của vaccine Astrazeneca ngừa Covid-19
Cụ thể, vừa qua tỉnh Khánh Hòa đã gửi Bộ Y tế đăng ký thử nghiệm vaccine Nanocovax, nhận phản hồi về việc hết hạn đăng ký và các hướng dẫn tiếp theo. Vì vậy, tỉnh gửi văn bản đề nghị được sử dụng thí điểm Nanocovax, nêu rõ mong muốn "góp phần đưa Nanocovax sớm đến tay người dân.
Trước đó, tỉnh Đồng Tháp cũng ban hành văn bản chỉ định một công ty trên địa bàn đặt mua 200.000 liều vaccine Nanocovax. Đây là lần đầu tiên một địa phương công bố đặt mua vaccine nội địa, đang thử nghiệm lâm sàng.
Ông Hồ Nhân, Chủ tịch Nanogen, cho biết đã tiếp nhận thông tin từ Đồng Tháp song hiện chưa thể cung ứng do vaccine chưa được cấp phép.
Nanocovax là vaccine Covid-19 do Công ty Cổ phần sinh học dược Nanogen nghiên cứu, phát triển. Vaccine đang thử nghiệm lâm sàng giai đoạn ba, do Học viện Quân y phối hợp với Viện Pasteur TP HCM thực hiện, tại 4 tỉnh gồm Hà Nội, Hưng Yên, Long An, Tiền Giang. Đây là vaccine Covid-19 đầu tiên của Việt Nam và là ứng viên sáng giá nhất.
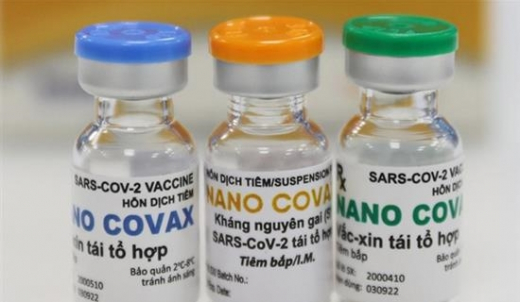
Bộ Y tế đã họp rà soát tiến độ thử nghiệm lâm sàng và đánh giá kết quả nghiên cứu giai đoạn một, hai, 3a và 3b của Nanocovax. Đại diện Nanogen cho biết kết quả đánh giá ở ngày thứ 42 sau khi tiêm liều một giai đoạn 3a trên 1.000 người tình nguyện, cho thấy 100% người tiêm vaccine có kháng thể trung hòa Surrogate trên ngưỡng 30%; 99,2% người chuyển đổi huyết thanh của kháng thể IgG kháng protein S gấp 4 lần so với nền (tức sinh miễn dịch chống virus).
Kháng thể trung hòa Surrogate là kết quả tạo kháng thể trung hòa với hạt nhựa giả virus, chỉ số này càng cao thì khả năng trung hòa virus càng cao. Kháng thể IgG kháng protein S, được hiểu là khả năng trung hòa virus của kháng thể sau khi tiêm vaccine.
Thứ trưởng Y tế Trần Văn Thuấn cho biết, Bộ Y tế đồng ý với chủ trương của các tỉnh tham gia thử nghiệm lâm sàng vaccine Nanocovax. Điều này sẽ giúp mở rộng phạm vi nghiên cứu, đánh giá được sự an toàn, hiệu quả của vaccine. Tuy nhiên, Bộ không ủng hộ tiêm vaccine chưa được cấp phép cho người dân.
Các tỉnh đăng ký tham gia thử nghiệm lâm sàng cần đúng quy trình nghiên cứu với nhiều bước khác nhau và phải được Hội đồng đạo đức (Bộ Y tế) phê duyệt. Khi thử nghiệm, cần đảm bảo thu thập, quản lý dữ liệu khoa học, có Sở Y tế các tỉnh, thành phố tham gia quản lý lượng mẫu lớn. Như vậy nghiên cứu thử nghiệm lâm sàng mới đảm bảo tin cậy, chính xác.
Bộ Y tế đã có công văn yêu cầu công ty Nanogen nộp đầy đủ hồ sơ dữ liệu thử nghiệm lâm sàng giai đoạn ba trên 12.000 người tình nguyện để Hội đồng đạo đức Bộ Y tế xem xét, thẩm định. Một khi Hội đồng đạo đức Bộ Y tế chưa xem xét hồ sơ thì Hội đồng tư vấn cấp giấy phép lưu hành thuốc và nguyên liệu làm thuốc chưa có cơ sở để xem xét, phê duyệt.
Phó giáo sư, tiến sĩ Lê Văn Truyền, Chủ tịch Hội đồng tư vấn cấp giấy đăng ký lưu hành thuốc, nguyên liệu làm thuốc của Bộ Y tế chia sẻ, theo điều 54 Luật Dược 2015 quy định "thuốc phải đăng ký trước khi lưu hành ở Việt Nam", có thể hiểu là thuốc và vaccine phải được Bộ Y tế cấp phép trước khi sử dụng cho người bệnh. Bên cạnh đó, việc đề xuất sử dụng vaccine chưa được cấp phép để thí điểm tiêm cho người dân là không phù hợp với quy định pháp luật hiện hành và cũng không phù hợp với y đức.
Hiện nay, làn sóng dịch bệnh Covid-19 quay trở lại và bùng phát mạnh tại nhiều tỉnh thành trên toàn quốc, làm tăng nhu cầu có vaccine để phòng, chống dịch bệnh. Nguồn cung vaccine thế giới khan hiếm khiến nguồn cung vaccine cho các nước bị ảnh hưởng.
Phó giáo sư Truyền cũng nhấn mạnh, trong giai đoạn này, Nanogen nhanh chóng tiến hành xử lý xong kết quả nghiên cứu theo yêu cầu của Bộ Y tế, trình Hội đồng đạo đức xem xét phê duyệt. Sau đó, Hội đồng tư vấn cấp phép sẽ xem xét hồ sơ, các nhà khoa học sẽ gấp rút làm việc trong thời gian ngắn nhất, để đề nghị Bộ trưởng Y tế cấp phép vaccine theo quy trình cấp phép sử dụng trong trường hợp khẩn cấp. Nếu thuận lợi, quý bốn năm nay, Việt Nam sẽ có vaccine phòng, chống Covid trong nước dùng cho người dân.
Cho đến thời điểm hiện tại, Việt Nam đã tiếp nhận hơn 16 triệu liều vaccine Covid-19 tính từ tháng 02 đến ngày 02/08, gồm vaccine AstraZeneca, Sputnik-V, Pfizer/BioNTech, Moderna, Vero Cell, trong tổng số 170 triệu liều đàm phán được.
Diệu Hương (T/h)


















